Materi IPA hari Kamis 7 Oktober 2021
KD 3.3 /BAB 3 KLASIFIKASI MATERI DAN PERUBAHANYA
Materi IPA Kelas 7 – Pada pembahasan bab 3 ini akan dibahas tentang Klasifikasi Materi dan Perubahannya memiliki materi yang cukup panjang, maka ringkasan materi ini dibagi menjadi 2 bagian. Bagian pertama ini membahas 3 sub materi penting yaitu :
1). Klasifikasi Materi,
2). Perbedaan Sifat Unsur, Senyawa, dan Campuran,
3). Pemisahan Campuran
Bagian ke-2 meliputi :
4) Perubahan Fisika dan kimia
5) Perbedaan Larutan Asam, Basa, dan Garam.
Materi IPA hari Kamis, 7 Oktober 2021
- KLASIFIKASI MATERI
Materi adalah sesuatu yang mempunyai massa dan dapat menempati ruang. Berdasarkan wujudnya, materi ada 3 yaitu : zat padat, cair dan gas. Berdasarkan komposisisnya, materi ada 2 yaitu : zat tunggal dan Campuran.
Perbedaan zat padat, cair dan gas
- Zat tunggal meliputi unsur dan senyawa,
Unsur adalah zat yang tidak dapat diuraikan lagi menjadi zat yang lebih sederhana melalui reaksi kimia biasa. Bagian terkecil dari unsur adalah atom. Unsur terdiri atas 1 jenis atom.
Unsur ada 3 macam yaitu :
1). Unsur logam contohnya besi, tembaga, emas, alumunium, perak, tembaga dan sebagainya. 2). Unsur nonlogam contohnya belerang, hidrogen, oksigen dan sebagainya.
3). Unsur semilogam contohnya germanium dan silikon.
- Setiap unsur dilambangkan dengan satu huruf , yaitu huruf awal dari nama latinnya contoh: Belerang nama latinya "Sulphur", lambang unsurnya ditulis S bukan B
- Huruf awal ditulis dengan huruf kapital atau huruf besar
- Untuk unsur yang memiliki huruf awal sama,diberikan tambahan satu huruf kecil dari nama unsur tersebut , contoh :
Contoh senyawa sederhana dan unsur pernyusunnya
Campuran adalah zat yang tersusun dari 2 atau lebih unsur dan senyawa, yang mana sifat dari unsur dan senyawa nya tidak hilang. Bedanya campuran dengan senyawa yaitu senyawa merupakan hasil dari reaksi kimia, sedangkan campuran bukan hasil dari reaksi kimia.
Ada 2 jenis campuran, yaitu :
1). Campuran Homogen adalah campuran yang komposisi zat penyusunnya merata. Contohnya air dengan garam, air dengan gula, dan sebagainya. Campuran homogen disebut juga dengan larutan. Larutan asam, basa dan garam juga merupakan campuran homogen.
2). Campuran Heterogen adalah campuran yang komposisi zat penyusunnya tidak merata. Contohnya air dengan kopi hitam, bensin dengan minyak tanah, dan sebagainya.
3. Pemisahan CampuranKebanyakan materi yang berada di alam ini tidak murni, melainkan masih berupa campuran. Seperti halnya udara yang kita hirup setiap hari sampai air laut yang berada di samudera. Udara sendiri terdiri dari beberapa macam zat seperti oksigen, nitrogen, uap air dan yang lainnya. Sedangkan air terdiri dari air, garam, dan zat yang lainnya.
Untuk memperoleh zat murni, kita harus memisahkannya dari campurannya. Prinsip pemisahan campuran didasarkan pada perbedaan sifat-sifat fisis zat penyusunnya, diataranya seperti wujud zat, ukuran partikel, titik leleh, titik didih, sifat magnetik, kelarutan, dan lain sebagainya. Berikut ini adalah beberapa metode dalam memisahkan campuran.
1. Filtrasi (penyaringan)
Filtrasi adalah metode pemisahan yang digunakan untuk memisahkan cairan dan padatan yang tidak larut dengan menggunakan penyaring (filter) berdasarkan perbedaan ukuran partikel. Sebagai contoh menyaring air yang bercampur pasir disaring dengan kertas saring sehingga pasir akan tertinggal di kertas saring.
2. Dekantasi
Dekantasi dapat digunakan sebagai salah satu alat alternatif selain filtrasi untuk memisahkan cairan dan padatan. Dekantasi dilakukan dengan cara menuang cairan secara perlahan-lahan, dengan demikian padatan akan tertinggal di dalam wadah tersebut. Metode jenis memang terbilang lebih cepat daripada filtrasi, namun hasilnya masih kurang efektif. Hasil akan menjadi lebih efektif bila ukuran zat padat jauh lebih besar, misalnya campuran air dengan kerikil.
3. Sentrifugasi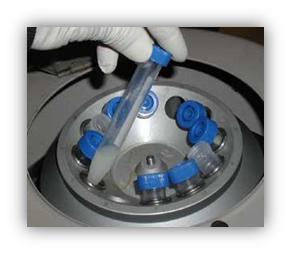
Metode jenis ini sering dilakukan sebagai pengganti filtrasi bila partikel padatan sangat halus dan jumlah campurannya lebih sedikit. Metide sentrifugasi digunakan secara luas untuk memisahkan sel-sel darah dan sel-sel darah putih dari plasma darah. Dalam hal ini, padatan adalah sel-sel darah dan akan mengumpul di dasar tabung reaksi, sedangkan plasma darah berupa cairan berada di bagian atas.
4. Evaporasi (evaporasi)
Jika garam dicampur dengan air akan terbentuk larutan, larutan tersebut tidak dapat dipisahkan dengan metode filtrasi maupun sentrifugasi. Metode yang digunakan untuk memisahkan zat padat yang terlarut dari larutannya disebut evaporasi. Sebagai contoh adalah larutan garam, larutan dipanaskan secara perlahan dengan uap air. Selama pemanasan, air dibiarkan menguap perlahan-perlahan hingga habis dan meninggalkan kristal garam sebagai residu.
5. Distilasi (penyulingan)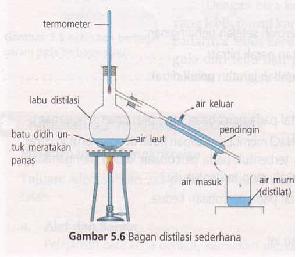
Distilasi adalah metode pemisahan campuran zat cair dari larutannya berdasarkan perbedaan titik didih. Jika larutan dipanaskan, maka komponen titik didihnya yang lebih rendah akan menguap terlebih dahulu. Dalam kehidupan sehari-hari proses penyulingan digunakan sebagai pemisahan air tawar dan air laut, pembuatan etanol atau alkhol, dan proses pemisahan minyak bumi.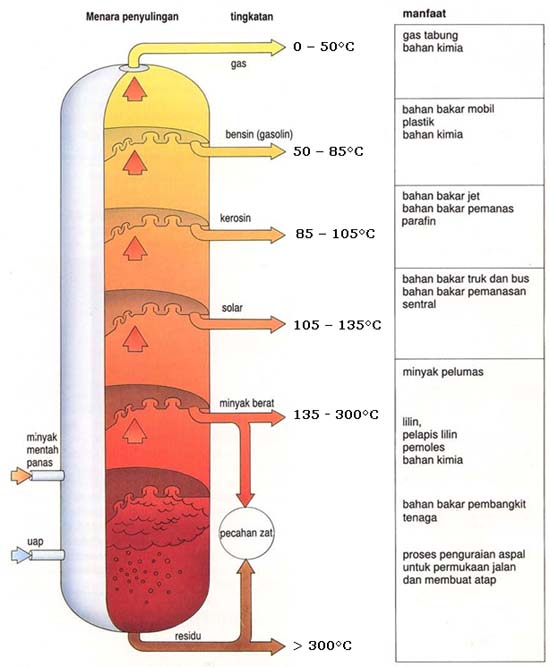
6. Corong pisah
Campuran dua jenis zat cair yang tidak saling melarutkan dapat dipisahkan dengan corong pisah lalu didiamkan selama beberapa saat sampai membentuk dua lapisan terpisah. Contohnya adalah seperti pemisahan air dengan minyak
7. Kromatografi
Contoh kromatografi pemisahan warna pada tinta
Kromatografi merupakan pemisahan campuran yang terjadi karena perbedaan kelarutan zat-zat dalam pelarut serta perbedaan penyerapan (adsorbsi) kertas terhadap zat-zat yang ingin dipisahkan. Suatu zat yang lebih dahulu larut dalam pelarut dan kurang terabsorbsi pada kertas akan bergerak lebih cepat.
Dalam kehidupan sehari-hari kromatografi berguna untuk :
- Menguji apakah bahan pewarna yang digunakan dalam makanan aman untuk dikonsumsi
- Menguji tinta yang digunakan pada pemalsuan dokumen seperti surat, cek dan giro
- Menguji apakah terdapat obat terlarang dalam urin atlet atau penyalahgunaan narkoba
- Memeriksa apakah pestisida yag terdapat pada sayuran atau buah-buahan masih dalam batas aman
8. Sublimasi

Sublimasi merupakan metode pemisahan campuran sesama zat padat berdasarkan perubahan wujud zat. Zat padat yang menyublim (berubah wujud menjadi gas atau sebaliknya) dapat dipisahkan dengan campurannya dengan zat padat yang tidak dapat menyublim menggunakan metode sublimasi. Contohnya seperti campuran iodin dengan garam dapat dipisahkan dengan cara pemanasan. Campuran dipanaskan di dalam wadah cawan yang ditutp dengan corong terbalik. Iodin akan menyublim dan menjadi uap, tapi pada saat menyentuh permukaan corong, uap iodin menyublim kembali menjadi padatan yang menempel pada permukaan corong sehingga dapat dipisahkan dengan padatan garam.
9 Ekstraksi (penyarian)
Pemisahan campuran dengan metode ekstraksi terjadi atas dasar perbedaan kelarutan zat terlarut di dalam pelarut yang berbeda. Ekstraksi sering dilakukan untuk mengambil sari dari suatu tumbuhan.
10 Rekristalisasi
Kristalisasi ialah pemisahan campuran dengan cara mengkristalkan atau mengendapkan zat terlarut dalam larutan yang tadinya berupa cairan juga. Biasanya kristalisasi ini menggunakan suhu rendah untuk membuat cairannya mengendap. Sedangkan rekristalisasi ialah suatu proses kristalisasi ulang. misalnya kita mendapatkan kristal, namun kristal tersebut belum murni. untuk mendapatkan kristal yang lebih murni dilakukan rekristalisasi. rekristalisasi dilakukan dengan cara melarutkan kristal dalam pelarut kemudian mengkristalkannya kembali
- Membuat rangkuman di buku catatan khusus IPA tentang klasifikasi materi, perbedaan unsur senyawa dan campuran serta serta pemisahan campuran
- Mengerjakan latihan soal dengan membuka link berikut 👇
- Perubahan fisika adalah perubahan suatu zat yang tidak disertai dengan pembentukan zat yang jenisnya baru. Contoh perubahan fisika, yaitu pencampuran gula ke dalam air membentuk larutan gula. Secara fisik gula berubah dari bentuk padat menjadi bentuk yang terlarut dalam air tetapi sifat gula masih sama, yaitu manis. Dalam perubahan wujud zat ada 6 jenis yaitu :
- Mencair adalah peristiwa perubahan wujud zat dari padat menjadi cair dengan mengandalkan energy panas. Contohnya mentega yang dipanaskan akan mencair atau lilin yang dipanaskan akan meleleh.
- Membeku adalah peristiwa perubahan wujud zat dari cair menjadi padat, dalam peristiwa ini zat melepaskan energy panas. Contohnya, air yang dimasukan dalam pembeku (freezer) akan menjadi es batu atau lelehan lilin yang dibiarkan akan mengeras.
- Mengkristal adalah peristiwa perubahan wujud zat dari gas menjadi padat, zat melepaskan energy panasnya. Contohnya berubahnya uap di udara menjadi salju.
- Menguap adalah peristiwa perubahan wujud zat dari cair menjadi gas, peristiwa ini memerlukan energy panas. Contohnya baju basah yang dijemur di bawah sinar matahari akan menjadi kering atau air yang direbus dan dibiarkan mendidih lama akan berkurang kuantitasnya karena menguap menjadi gas.
- Menyublim adalah peristiwa perubahan zat dari padat menjadi gas, dimana zat memerlukan energy panas. Contohnya kapur barus yang disimpan dalam lemari pakaian lama-lama akan habis.
- Mengembun adalah peristiwa perubahan wujud zat dari gas menjadi cair, dalam peristiwa ini zat melepaskan energy panas. Contohnya rumpu dan tanaman yang dekat dengan tanah menjadi basah pada pagi atau butiran air di bagian luar gelas yang berisi es.
b. Perubahan Kimia
- Perubahan kimia adalah perubahan suatu zat yang menghasilkan zat baru. Perubahan kimia ini bersifat permanen yang artinya zat hasil terbentuknya tidak dapat diubah lagi menjadi zat asalnya. Contohnya adalah kertas terbakar, petasan meledak, singkong menjadi tape, besi berkarat, dan pembusukan makanan.
- Perubahan kimia disebut juga dengan reaksi kimia, dimana terdapat dua istilah yang digunakan yaitu zat semula dinamakan reaktan atau pereaksi dan zat yang terbentuk dinamakan hasil reaksi atau produk reaksi. Contohnya jika kayu dibakar akan menghasilkan arang kayu, kayu dinamakan pereaksi dana rang kayu dinamakan hasil reaksi.
Terjadinya reaksi kimia dapat dilihat dari ciri-ciri yang menyertai perubahan zat tersebut yaitu:
- Perubahan warna : suatu zat mempunyai warna tertentu tergantung komposisi dan kandungan unsur atau senyawa dalam zat tersebut. Contohnya, sendok logam yang ditempatkan di atas nyala api maka akan terbentuk warna hitam dari asap yang mengandung karbon atau arang.
- Perubahan suhu : reaksi kimia terjadi karena adanya perubahan energy yang menyertai reaksi kimia. Ada dua perubahan suhu yang menyertai perubahan kimia yaitu kalor yang dilepaskan dan kalor yang dibutuhkan dalam perubahan kimia.Berdasarkan perubahan suhu yang terjadi, reaksi kimia dikelompokan menjadi dua, yaitu reaksi eksoterm (pembebasan energi panas) dan endoterm (penyerapan energi panas).
- Pembentukan endapan : suatu zat yang sukar larut dalam pelarut air. Contohnya reaksi antara perak nitrat dengan natrium klorida yang menghasilkan endapan perak klorida yang berwarna putih.
- Pembentukan gas : beberapa perubahan kimia ada yang menghasilkan gas. Contohnya, reaksi pembakaran yang menghasilkan gas CO2 atau reaksi pembusukan menghasilkan gas-gas yang berbau menyengat seperti gas ammonia.(https://www.kelaspintar.id/blog/tips-pintar/pengertian-perubahan-fisika-dan-kimia-berserta-contohnya-4494/)
- Reversibel = kembali semula
- Irrevesibel = tidak kembali semula
Sifat suatu zat dibedakan menjadi dua, yaitu secara fisika dan kimia. Kita bahas satu-persatu, ya.
Sifat Fisika Zat
Sifat fisika suatu zat berkaitan dengan penampilan atau keadaan fisis zat tersebut, di antaranya:
1) Wujud zat
Masih ingat dengan percobaan di atas? Dari percobaan di atas tadi kita jadi tahu ya kalau wujud suatu zat terbagi menjadi tiga, yaitu padat, cair, dan gas. Nah, wujud zat juga dapat berubah ke wujud lain. Apa aja sih bentuk perubahannya? Eits! Tahan dulu ya. Kita akan membahasnya di bagian perubahan bentuk zat. Jadi, pastikan kamu membaca artikel ini sampai tuntas.
2) Warna
Warna merupakan salah satu sifat fisika yang dapat kamu amati secara langsung, nih. Setiap zat memiliki warna yang berbeda-beda. Hal ini yang membedakan antara zat satu dengan zat yang lainnya. Contohnya, batu bara berwarna hitam, kayu berwarna coklat, besi berwarna abu-abu keperakan, dan masih banyak lagi.
3) Kelarutan
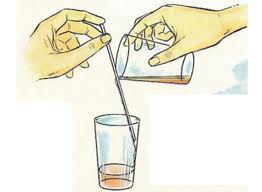
Kelarutan adalah kemampuan suatu zat untuk larut (bercampur) dalam pelarut. Air merupakan pelarut untuk zat-zat terlarut. Apakah semua zat dapat larut? Jawabannya, enggak. Kita ambil dua contoh kasus, misalkan ada dua gelas berisi air. Gelas pertama, kamu campur dengan garam, sedangkan gelas kedua kamu campur dengan minyak. Lalu, aduk dan lihat perbedaannya. Hasilnya, garam pada gelas pertama lama kelamaan akan hilang karena bercampur (larut) dengan air. Sementara itu, minyak pada gelas kedua tidak dapat larut dengan air, sehingga membentuk dua lapisan terpisah.
4) Daya hantar listrik
Suatu zat atau benda digolongkan menjadi dua berdasarkan kemampuannya dalam menghantarkan listrik, yaitu konduktor dan isolator. Benda yang dapat menghantarkan listrik dengan baik disebut konduktor. Contohnya benda-benda yang terbuat dari logam, seperti besi, alumunium, tembaga, kawat, dsb. Sementara itu, benda yang tidak dapat menghantarkan listrik disebut isolator. Contohnya, benda-benda non-logam, seperti kain, plastik, karet, kayu, dsb.
5) Kemagnetan
Berdasarkan sifat kemagnetannya, benda juga digolongkan menjadi dua, yaitu benda magnetik dan benda non-magnetik. Benda magnetik adalah benda yang dapat ditarik oleh magnet, sedangkan benda non-magnetik adalah benda yang tidak dapat ditarik oleh magnet. Umumnya, benda-benda logam akan memiliki sifat magnetik dan kebalikannya, benda non-logam akan memiliki sifat non-magnetik.
Sifat Kimia Zat
Sifat kimia suatu zat berkaitan dengan perubahan kimia yang dialami oleh zat tersebut, antara lain:
1) Mudah terbakar
Coba sebutkan benda apa aja yang memiliki sifat mudah terbakar? Kertas, kayu, kain, bensin, minyak tanah, gas elpiji, dan masih banyak lagi, ya. Umumnya, benda-benda tersebut terbakar karena adanya interaksi langsung dengan api. Bahan-bahan yang mudah terbakar merupakan bahan yang mudah bereaksi dengan oksigen dan menimbulkan kebakaran. Bahkan, jika reaksi kebakaran yang ditimbulkan amat cepat, hal ini dapat menyebabkan ledakan, loh.
2) Busuk dan asam
Makanan dan minuman yang dibiarkan terlalu lama akan membusuk atau basi. Hal ini terjadi karena adanya reaksi kimia antara zat-zat pada makanan dan minuman tersebut dengan oksigen (udara). Oleh sebab itu, agar makanan dan minuman jadi lebih awet, kamu bisa memanaskannya kembali atau menyimpannya ke dalam kulkas.
3) Berkarat
Reaksi antara logam dengan air dan oksigen dapat menimbulkan karat pada logam tersebut. Oleh karena itu, sesuatu yang terbuat dari logam, seperti besi dan seng akan mudah berkarat bila terkena air dan udara pada waktu yang cukup lama. Contohnya pada pagar besi. Siapa yang pagar rumahnya terbuat dari besi? Kalau kamu perhatikan, seiring waktu, pagar itu akan berkarat. Nah, biasanya, pagar besi selalu dilapisi cat untuk memperlambat proses pengaratan.
4) Mudah meledak
Interaksi antara zat yang mudah meledak dengan udara, api, atau cahaya matahari dapat menimbulkan ledakan. Pernah nggak kamu membaca peringatan “simpan di tempat yang terhindar dari sinar matahari” pada kemasan botol parfum? Hayo, kira-kira apa alasannya, ya? Ternyata, parfum yang sering kamu pakai itu mengandung bahan kimia yang mudah terbakar, lho. Jadi, harus disimpan pada suhu ruangan yang rendah. Jika terlalu banyak terkena sinar matahari, hati-hati, botol parfum bisa meledak.
5) Beracun
Beberapa zat bisa berubah menjadi sangat beracun ketika mengalami reaksi kimia tertentu. Contohnya adalah gas karbon monoksida (CO). Gas ini dihasilkan dari pembakaran tidak sempurna dari atom karbon. Gas karbon monoksida sulit sekali dideteksi karena wujudnya yang tidak berwarna dan tidak berbau. Apabila seseorang menghirup gas karbon monoksida, maka akan menyebabkan aliran oksigen dalam darah tidak lancar, gagal bernafas, hingga kematian. Wow, seram banget nggak, sih?
Tidak semua massa jenis benda harus diukur dengan cara demikian. Khusus untuk zat zat cair, massa jenisnya dapat diukur dengan menggunakan alat yang disebut hidrometer.
Hidrometer adalah alat ukur massa jenis zat cair secara langsung. Hidrometer berupa botol kecil yang panjang dengan garis-garis skala disepanjang botol itu. Ketika hidrometer dimasukkan kedalam zat cair, maka hidrometer akan terapung dengan posisi berdiri. Permukaan zat cair akan menunjukkan besar massa jenis zat cair tersebut.
mengapa kapal laut dapat terapung sedangkan uang logam tenggelam?. Memang kapal terbuat dari baja dan bahan-bahan lain yang massa jenisnya besar, tetapi secara keseluruhan massa jenis kapal menjadi kecil (lebih kecil dari massa jenis air laut) karena volume kapal yang masuk kedalam air laut dibuat sangat besar. Sedangkan uang logam, tidak ada rongganya sama sekali sehingga massa jenis uang logam sama dengan massa jenis bahan uang logam tersebut. Itulah sebabnya uang logam itu tenggelam dalam air laut, sedangkan kapal laut dapat terapung.
- Massa jenis benda adalah perbandingan antara massa suatu benda dengan volume benda tersebut. Massa jenis benda menunjukkan tingkat kerapatan molekul benda tersebut.
- Satuan massa jenis dalam sistem cgs adalah g/cm3, dan dalam sistem MKS / Sistem Internasional adalah kg/m3.
- Massa jenis zat cair dapat diukur secara langsung dengan hidrometer.
- Massa jenis benda merupakan ciri khas benda tersebut.
Contoh cara mengukur massa jenis suatu benda
https://blog.ruangguru.com/sifat-dan-perubahan-bentuk-zat
5. Larutan asam, basa dan garam
Pengujian larutan asam dapat menggunakan cara yaitu : kertas lakmus merah, kertas lakmus biru, metil merah, metil jingga, dan mahkota bunga jika salah satu dari mereka dicelupkan kedalam larutan asam, makan akan berubah warna menjadi merah. Apabila diukur menggunakan pH meter akan menunjukkan pH dibawah 7.Ciri-ciri larutan basa:
!) Mempunyai rasa agak pahit (tidak boleh dicicipi)
2). Terasa licin di kulit
3). Mengubah lakmus merah menjadi biru.
Contoh larutan basa dalam kehidupan sehari-hari

Pengujian larutan basa dapat menggunakan cara :
- Kertas lakmus merah dan lakmus biru dicelupkan pada larutan basa akan berubah warna menjadi biru
- Metil merah dan metil jingga direaksikan dengan larutan basa akan berwarna kuning
- Fenoftalein direaksikan dengan larutan basa akan berwarna merah
- Mahkota bunga direaksikan dengan larutan basa akan berwarna biru
Garam adalah gabungan antara asam dan basa hasil dari reaksi netralisasi. Garam yang sering digunakan adalah garam dapur atau natrium klorida (NaCl). Contoh reaksi netralisasi yaitu :
HCl + NaOH NaCl + O
Asam klorida + natrium hidroksida menjadi garam natrium klorida + air
Larutan asam, basa, dan garam juga dapat dibedakan dengan derajat keasaman (pH). Jika larutan bersifat asam maka mempunyai pH <7, jika bersifat garam atau netral maka pH nya adalah 7, dan jika bersifat basa maka mempunyai pH >7.


Berikut contoh indikator alami untuk menguji larutan asam, basa dan garam (asambaga)

Untuk lebih jelasnya silahkan menyaksikan dengan seksama video berikut ini tentang Klasifikasi Materi dan Perubahannya👇
https://www.youtube.com/watch?v=VmlYkIRKVJY
Setelah kalian mempelajari materi dan menyimak tayangan video tentang klasifikasi materi dan perubahanya, maka tugasmu hari ini Kamis, 14 Oktober 2021 antara lain:
- Membuat rangkuman di buku catatan khusus IPA tentang : Sifat fisika dan kimia zat, Perubahan fisika dan kimia serta larutan asam, basa dan garam
- Memngerjakan latihan soal , boleh membuka buku catatan /paket dengan membuka link berikut ini: https://forms.gle/MDGsY8tgShkhxQe46






































YUNA ISTI HANI
BalasHapusVII-D/32
SIAP MENGERJAKAN
AMIRA NABILA PUTRI KUSINDARJI
BalasHapusVIIC/4
SIAP MENGERJAKAN
ANITA RAHMAWATI
BalasHapusVIIA/04
SIAP MENGERJAKAN
NADHIFA YUMNA RIUNAS
BalasHapusVIIE
22
SIAP MENGERJAKAN
NUR SIWAN BAYANI
BalasHapus23/7D
SIAP MENGERJAKAN
ABIYAN ANWAR KURNIAWAN
BalasHapusVII C / 1
Siap mengerjakan
DIEGY ABIAN DEVRA
BalasHapus7c/12
Siap mengerjakan tugas
YIESHA NIAR RAMADHANI VII C/32
BalasHapusSiap mengerjakan tugas
NUR SIWAN BAYANI
BalasHapus23
7D
SIAP MENGERJAKAN
KHOIRUNNISA MUFLIHAH RAHMADINA
BalasHapus7D/13
SIAP MENGERJAKAN
RADITYA ADI BRATANDARU
BalasHapusVIID/24
SIAP MENGERJAKAN
LUTFI NIKMATUL KHASANAH
BalasHapusVIIC/19
SIAP MENGERJAKAN
DIEGY ABIAN DEVRA
BalasHapusVII C/12
SIAP MENGERJAKAN TUGAS